

1. Acide chlorhydrique et sels de chlorure
a. Acide chlorhydrique
Un des acides inorganiques les plus classiques, il présente une bonne solubilité pour les oxydes de fer et les minéraux argileux. Il est largement utilisé en raison de son faible prix et de son effet évident et intuitif. Que ce soit pour le décapage afin d'éliminer la peau jaune dans la plaque de quartz, ou pour le décapage de sable de haute pureté, l'acide chlorhydrique est privilégié.
Le traitement des eaux usées contenant de l'acide chlorhydrique est relativement simple. La neutralisation de la solution avec une base jusqu'à la neutralité et la re-précipitation peuvent répondre à la norme nationale de rejet. Cependant, parmi les cas de protection de l'environnement liés à la pollution acide dans divers endroits, la pollution des eaux usées contenant de l'acide chlorhydrique est la plus courante.
Pourquoi ?
La neutralisation des eaux usées acides nécessite une consommation de bases. En prenant l'exemple de la chaux vive, qui est la plus couramment utilisée, selon l'équilibre chimique, le liquide de déchet produit par une tonne d'acide chlorhydrique industriel à 31 % consomme théoriquement environ 0,25 tonne de chaux vive. En réalité, comme la chaux vive n'est pas entièrement dissoute, si 50 % de la chaux vive participe à la réaction, environ 0,5 tonne de chaux vive est consommée pour le liquide de déchet produit par une tonne d'acide chlorhydrique industriel. Le prix d'une tonne d'acide chlorhydrique industriel est de 100 à 400 yuans, le prix moyen de référence étant de 300 yuans ; le prix d'une tonne de chaux vive est de 400 à 1000 yuans, avec un prix moyen de référence de 700 yuans. Nous pouvons alors constater que le coût d'utilisation d'une tonne d'acide chlorhydrique est de 300 yuans, le coût de la chaux pour le traitement des eaux usées est de 350 yuans, et le coût de traitement des eaux usées a dépassé le coût d'utilisation de l'acide chlorhydrique. Certaines entreprises non conformes, d'une part, n'ont pas d'installations de traitement des eaux usées, et d'autre part, sont réticentes à supporter des coûts plus élevés, ce qui entraîne des incidents fréquents de pollution par décharge directe des acides usés.
Après tout, Marx a dit : « Pour 100 % de profit, le capital n'hésite pas à piétiner toutes les lois humaines ».
b. Sels de chlorure
Les sels de chlorure courants, tels que le chlorure de sodium, le chlorure de potassium, le chlorure de lithium, le chlorure de calcium et le chlorure de magnésium, peuvent être utilisés pour le dopage et la purification du sable de quartz, et peuvent également être utilisés pour la torréfaction par chloruration et le blanchiment dans des minéraux non métalliques tels que le kaolin.
Certaines littérature mentionnent la chloruration et la purification du sable de quartz avec du chlorure d'ammonium, de l'hydrogène chloré, du chlore ou du tétrachlorure de carbone.
2. Acide sulfurique et sulfate
Acide inorganique binaire à forte propriété oxydante et à point d'ébullition élevé. Le point d'ébullition de l'acide sulfurique concentré est de 338 °C, et il est non volatil dans des conditions normales, il n'est donc pas aussi largement utilisé que l'acide chlorhydrique dans les applications nécessitant un traitement de brouillard acide. L'avantage de son point d'ébullition élevé est que les minéraux peuvent être traités avant d'atteindre le point d'ébullition (comme autour de 300 °C) sans utiliser de récipient sous haute pression. De telles conditions extrêmes peuvent décomposer certains minéraux qui ne peuvent pas être dissous par de l'acide chlorhydrique. Bien sûr, cette situation impose des exigences élevées en matière de matériaux et de protection de la sécurité, ce qui est rarement observé dans la production réelle, mais plus dans les laboratoires.
Certaines littératures mentionnent l'utilisation de sels d'acide sulfurique et la calcination du sable de quartz pour réduire la teneur en titane du sable de quartz. Le traitement avec des sels d'ammonium d'acide sulfurique réduit la teneur en fer du sable de quartz.
Le traitement des eaux usées acides de l'acide sulfurique et des sulfates est le même que celui des eaux usées de l'acide chlorhydrique, qui peut être neutralisé avec de l'alcali.
3. Acide hydrofluorique et sels fluorés
L'acide hydrofluorique, acide faible monobasique, avec sa capacité de super complexité, est devenu un grand tueur pour la purification du sable de quartz. Dans certaines conditions, l'acide hydrofluorique réagit avec la plupart des minéraux d'impureté, y compris le sable de quartz. Par conséquent, lorsque la concentration d'acide hydrofluorique est trop élevée, il est nécessaire de faire attention à la perte de sable de quartz. Les acides mixtes d'acide hydrofluorique et d'acide chlorhydrique, d'acide sulfurique ou d'acide nitrique sont des systèmes d'acide mixte couramment utilisés. Dans le domaine des champs pétrolifères, le graphite, le carbure de silicium et d'autres minéraux non métalliques adoptent un système d'acide mixte contenant de l'acide hydrofluorique.
Le rôle des sels fluorés dans les systèmes contenant des acides est similaire à celui de l'acide hydrofluorique. Les sels fluorés sont également utilisés comme dopants.
Les perles produites par la civilisation industrielle humaine sont indissociables de l'existence de l'acide hydrofluorique. Dans l'industrie des semi-conducteurs, l'acide hydrofluorique est principalement utilisé pour nettoyer la surface des plaquettes, ou dans le processus de nettoyage et de gravure lors du traitement des puces. Dans l'industrie solaire, l'acide hydrofluorique est utilisé dans des processus tels que le nettoyage et la gravure de la surface des puces. Dans l'industrie des panneaux, l'acide hydrofluorique est utilisé pour nettoyer les substrats en verre et pour graver le nitrure de silicium et le dioxyde de silicium. Cependant, dans l'industrie du sable de quartz de haute pureté, certaines personnes essaient de trouver une solution « sans fluor » ou même « sans acide ». Est-ce scientifique ?
En plus de la neutralisation alcaline, le point le plus important du traitement des eaux usées d'acide hydrofluorique est de réduire la concentration des ions fluorure dans la plage autorisée par la norme nationale. Le processus de traitement global n'est pas compliqué, et les entreprises régulières sont capables de traiter les eaux usées d'acide hydrofluorique. Cependant, certaines petites entreprises dispersées n'ont pas d'installations professionnelles de traitement des eaux usées et ne sont pas disposées à augmenter le coût de traitement, et le rejet direct des eaux usées cause une pollution environnementale. Si les eaux usées sont directement rejetées sans traitement, il est facile de provoquer un excès de fluor dans la zone aquatique, ce qui est également la principale raison de la décoloration du fluor dans certaines régions.
4. Phosphate et phosphates
Acide ternaire moyennement fort, point d'ébullition 261 ℃ (décomposition). L'acide phosphorique concentré et chaud peut décomposer la plupart des minéraux, tels que la chromite, le rutile, l'ilménite, etc., et peut également réagir avec la silice pour former des hétéropolyanions. L'acide phosphorique est le seul acide autre que l'acide hydrofluorique qui peut réagir avec le quartz.
Le sel normal et le sel acide de l'acide phosphorique peuvent également être observés dans les expériences de corrosion des matériaux en quartz.
Le traitement des eaux usées de l'acide phosphorique et des phosphates doit d'abord être neutralisé par de l'alcali, puis la concentration des phosphates doit être réduite à la plage autorisée par la norme nationale.
5. Acide nitrique et nitrates
L'acide nitrique est un acide fort inorganique avec de fortes propriétés oxydantes. Pour certaines impuretés minérales réductrices, l'effet des systèmes acides conventionnels est limité, certaines réactions ne se produisent pas, et certaines réactions qui sont chimiquement thermodynamiquement faisables sont cinétiquement entravées. À ce moment-là, si un oxydant fort est impliqué, la réaction peut être réalisée et la vitesse de réaction peut être considérablement accélérée. Et parce que les nitrates ont généralement une solubilité plus élevée, l'ajout d'acide nitrique empêche la précipitation des produits de réaction. L'utilisation mixte de l'acide nitrique et d'autres systèmes acides est appropriée pour le traitement du sable de quartz contenant des minéraux réducteurs.
Le rôle du nitrate dans les systèmes contenant de l'acide est similaire à celui de l'acide nitrique. Le nitrate est également utilisé comme dopant.
Dans le traitement des eaux usées contenant de l'acide nitrique et des nitrates, en plus de la neutralisation avec des bases, des mesures doivent également être prises pour réduire la teneur en azote ammoniacal dans les eaux usées.
1. Acide oxalique
L'organe binaire est fort, et son acidité est une acide moyennement fort, ce qui en fait un acide fort parmi les acides organiques. L'oxalate a un fort effet de coordination et est un chélateur métallique efficace. Dans l'expérience d'élimination du fer du sable de quartz, l'utilisation de l'acide oxalique seul, ou la combinaison de l'acide oxalique et des ondes ultrasonores, ou la combinaison de l'acide oxalique et d'autres systèmes acides, peut aboutir à un meilleur effet d'élimination du fer et de blanchiment. Il existe également de nombreux rapports mentionnant que l'acide oxalique est utilisé dans la purification et le blanchiment des minéraux non métalliques tels que le kaolin. De plus, la quantité d'acide oxalique n'a pas besoin d'être aussi grande que celle des acides inorganiques traditionnels tels que l'acide chlorhydrique, et ne doit pas dépasser 5 % pour atteindre l'effet maximum de conservation. L'oxalate se combinera avec les ions calcium et magnésium pour former des précipités de faible solubilité, donc l'acide oxalique a certaines limitations lorsqu'il s'agit de minéraux avec une forte teneur en métaux alcalino-terreux.
Dans les eaux usées d'acide oxalique, en plus de l'influence de l'acide, la présence d'oxalate en tant que matière organique augmentera également considérablement la demande chimique en oxygène du corps aquatique. Par conséquent, le traitement à la chaux est la solution privilégiée. En plus de neutraliser l'acidité, l'acide oxalique peut également être précipité pour réduire considérablement la teneur résiduelle en oxalate.

2. Acide citrique et citrate de sodium
L'acide citrique est un composé d'acide tricarboxylique et est un acide organique important. L'acide citrique est plus faible que l'acide oxalique, mais c'est un acide fort parmi les acides organiques. L'acide citrique et ses sels ont une forte capacité de chélation dans la plage acide, et peuvent chélater la plupart des ions métalliques trivalents et divalents. La plage d'utilisation appropriée est pH=4~8. Le chélate formé par l'acide citrique et l'ion fer a une faible solubilité et formera un précipité dans l'eau. Afin d'augmenter sa solubilité, une quantité appropriée de sel d'ammonium est ajoutée pour former un composé avec une solubilité plus élevée.
La plus grande difficulté dans le traitement des eaux usées d'acide citrique et d'autres composés organiques est la réduction de la demande chimique en oxygène. Une grande quantité de matière organique entre dans les eaux usées, ce qui fait exploser la demande chimique en oxygène. La réduction de la demande chimique en oxygène nécessite un équipement et des sites professionnels, tels que des bassins d'oxydation chimique et des bassins d'oxydation biologique, dont l'investissement en capital et la difficulté de traitement sont bien plus importants que ceux des installations de neutralisation acide-base.
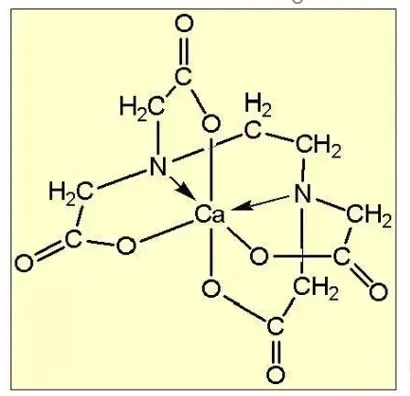
3. EDTA (acide éthylènediaminetétraacétique) et son sel de sodium
L'EDTA et son sel de sodium sont des agents complexants importants, qui possèdent une large gamme de propriétés de coordination et peuvent former des chélates stables avec presque tous les ions métalliques. Il est utilisé dans un environnement neutre et légèrement alcalin, et a une faible capacité de corrosion. Il est adapté pour l'élimination des minéraux argileux et des impuretés en oxyde de fer en film mince.
4. Autres agents complexants
Tels que l'acide acétique, l'acide salicylique, l'acide polyphosphonique organique, etc., l'acidité est relativement faible, mais la capacité de complexation est exceptionnelle, et il peut être utilisé comme agent complexant.
Il est encore inconnu s'il existe une meilleure solution pour le traitement chimique du sable de quartz. Et chaque substance a des avantages et des inconvénients correspondants, généralement plusieurs substances sont mélangées pour obtenir le meilleur effet. L'effet d'utilisation combinée de diverses substances et si le schéma médicamenteux correspond à l'objectif du traitement sont tous des facteurs que nous devons prendre en compte lors du traitement du sable de quartz. J'espère que chacun pourra s'adapter aux conditions locales et utiliser le schéma médicamenteux le plus adapté.
Pour en savoir plus sur nos produits et solutions, veuillez remplir le formulaire ci-dessous et l'un de nos experts vous répondra sous peu
Projet de flottation de l'or de 3000 TPD dans la province du Shandong
Flottation de minerai de lithium de 2500 TPD au Sichuan
Fax : (+86) 021-60870195
Adresse :No.2555, Route Xiupu, Pudong, Shanghai
Droits d'auteur © 2023.Prominer (Shanghai) Mining Technology Co., Ltd.
